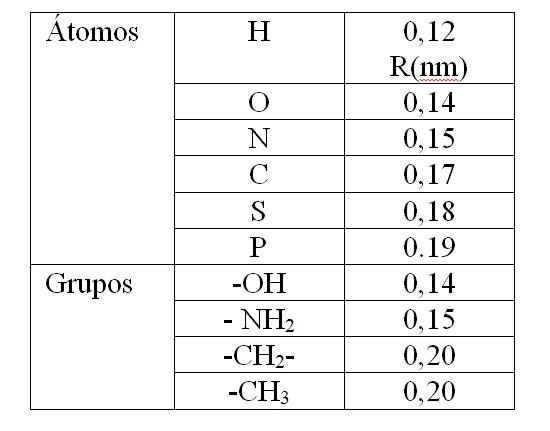
El administrador recopila información Enlace Por Fuerzas De Van Der Waals Ejemplos.
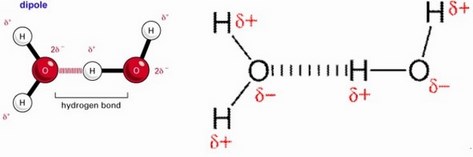
El enlace de van der waals es un tipo de enlace intermolecular en el que las moléculas polares se unen unas con otras por la existencia de dipolos. Son las llamadas interacciones dipolo dipolo fuerzas de keeson.
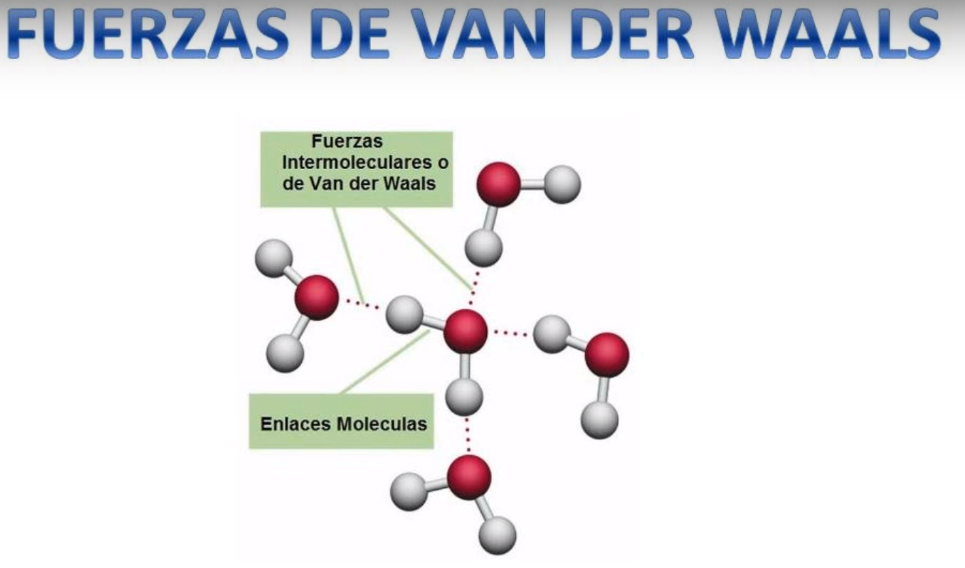
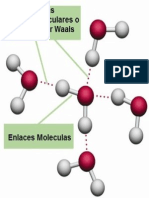
Otro ejemplo de fuerzas de van der waals es la que se dan en moléculas suspendidas en el agua.

Enlace por fuerzas de van der waals ejemplos.
No es difícil de entender que existirán interacciones de este tipo entre las moléculas polares hcl por ejemplo.
Las fuerzas de van der waals son fuerzas intermoleculares de naturaleza eléctrica que pueden ser atractivas o repulsivas.
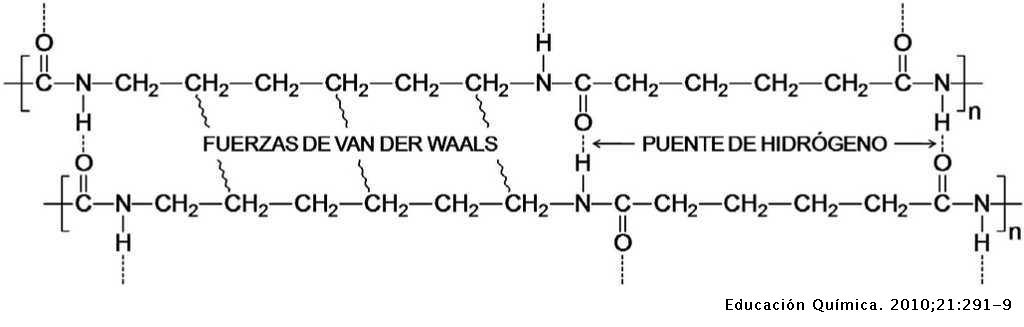
Sabemos porque la nafta es un líquido el metano es gas y el polietileno que se representa como un polímero compuesto por c y por h nada más es un sólido.
De hecho las fuerzas de van der waals son las fuerzas atractivas o repulsivas entre moléculas o entre partes de una misma molécula distintas a aquellas debidas a un enlace covalente iónico o metálico.
En la química se le da alusión a una sub rama de la fisicoquímica denominada interacción o fuerzas de van der waals que gracias a ellas podemos dar explicación a la adhesión el rozamiento la difusión la tensión superficial y la viscosidad de distintos compuestos orgánicos.
Enlaces por fuerzas de van der waals.
Asociadas con energías entre 04 y 40 kjmol generalmente quedan enmascaradas por las fuerzas covalentes más fuertes con energías típicas de 400.
De todas las fuerzas que desempeñan un papel a nivel molecular las llamadas fuerzas de van der waals son sin duda las más débiles pero probablemente las más universales.
Incluyen a atracciones entre átomos moléculas y superficies fuera de los enlaces normales.
Enlace de van der waals es un tipo de enlace intermolecular en el que las moléculas polares se unen unas con otras por la existencia de dipolos.
Enlace de van der waals.
Son fuerzas mucho más débiles que los enlaces moleculares del orden de 100 veces menores a los enlaces iónico covalente y metálico pero fundamentales para explicar muchos fenómenos.
Las fuerzas de van der waals son muy débiles cuando las moléculas son eléctricamente simétricas es decir que tienen momento dipolar nulo no polares o apolares como ocurre por ejemplo en las moléculas monoatómicas de los gases nobles así como en las moléculas diatómicas homonucleares h 2 n 2 f 2.
Son fuerzas mucho más débiles que los enlaces moleculares del orden de 100 veces menores a los enlaces iónico covalente y metálico pero fundamentales para explicar muchos fenómenos.
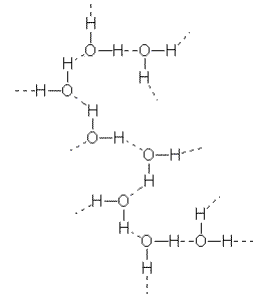
Fuerzas de van der waals enlaces de hidrógeno la fuerzas de van der waals son fuerzas de tipo electrostático entre cargas de signo distinto.
Esto sucede gracias a que se dan fuerzas electroestáticas entre dichas moléculas que generan las fuerzas de van der waals.
A la totalidad de estas fuerzas intermoleculares se las conoce como fuerzas de van der waals nombre que hace homenaje al físico holandés johannes diderik van der waals 1837 1923 quien fuera el primero en proponer sus efectos en las ecuaciones de estado de un gas conocida como ecuación de van der waals.
Hay una interacción entre las superficies de las moléculas o átomos distinta en esencia de los enlaces iónicos covalentes y metálicos que se forman en el interior de las moléculas.
Eso es lo que podemos compartir enlace por fuerzas de van der waals ejemplos. El administrador del blog Nuevo Ejemplo 10 January 2019 también recopila otras imágenes relacionadas con los enlace por fuerzas de van der waals ejemplos a continuación.
Eso es lo que el administrador puede dar acerca de enlace por fuerzas de van der waals ejemplos. Gracias por visitar el sitio Nuevo Ejemplo 10 January 2019.